La carne cultivada es cara, pero los costos están disminuyendo. ¿El mayor obstáculo? El medio de cultivo, que puede costar cientos de libras por litro. Para competir con la carne tradicional, los precios deben caer a £1 por litro o menos. Tres estrategias están impulsando este cambio:
- Ingeniería de Líneas Celulares: Ajustar las células animales para reducir las necesidades de nutrientes y crecer de manera eficiente.
- Optimización de Medios: Reemplazar ingredientes costosos de grado farmacéutico por alternativas más baratas de grado alimenticio.
- Mejoras en Bioreactores: Escalar la producción con sistemas más grandes y eficientes.
Cada enfoque aborda un desafío único, pero su progreso combinado es clave para hacer que la carne cultivada sea asequible. ¿El objetivo? Acercar los precios a la carne convencional, haciéndola accesible para todos.
Ingeniería de Líneas Celulares para Carne Cultivada y Agricultura Celular Sostenible #culturedmeat
1. Ingeniería de líneas celulares
La ingeniería de líneas celulares ofrece una forma ingeniosa de reducir los costos de nutrientes al modificar células animales para que produzcan sus propios factores de crecimiento. En lugar de añadir constantemente factores de crecimiento costosos al medio de cultivo, los científicos están permitiendo que las células creen estos nutrientes por sí mismas a través de señalización autocrina.
En 2024, Andrew J. Stout y su equipo en la Universidad de Tufts lograron modificar con éxito células musculares bovinas para que produjeran su propio FGF2 [4][2]. Kevin Kayser, Director Científico en Upside Foods, resumió el enfoque perfectamente:
"Construyamos un proceso y luego seleccionemos una línea celular que haga lo que queremos que haga. Va a ser mucho más trabajo inicial, pero al final se traducirá en un mejor costo" [1].
Potencial de Reducción de Costos
Las proteínas recombinantes y los factores de crecimiento son los principales impulsores de costos en el proceso de producción [3]. Al diseñar células para generar sus propios factores de crecimiento, las empresas pueden eliminar la necesidad de suplementos externos costosos, algo que de otro modo requeriría una reducción de costos cercana al 99% para hacer que la carne cultivada sea comercialmente viable [5]. Además, modificar las células para crecer en suspensión, en lugar de requerir una superficie, permite el uso de bioreactores de tanque agitado masivos (algunos que superan los 20,000 litros), aumentando significativamente la eficiencia de producción [2].
Plazo de Implementación
Este enfoque no está exento de desafíos.Desarrollar y caracterizar una nueva línea celular típicamente toma de 6 a 18 meses [3], lo que contrasta fuertemente con el ciclo de producción mucho más corto de solo 2 a 8 semanas, desde el banco celular hasta la cosecha [3]. Para 2023, casi la mitad de las empresas de carne cultivada ya estaban explorando la ingeniería genética para fines de investigación o comerciales [3], posicionando a la industria para refinar aún más las estrategias de ahorro de costos.
Desafíos Técnicos
Aún hay obstáculos que superar. Mantener la estabilidad genómica y lograr la inmortalización para la proliferación celular indefinida - mientras se asegura que las células aún puedan diferenciarse adecuadamente - sigue siendo un desafío difícil de resolver [4][3]. Además, la disponibilidad de líneas celulares con las características adecuadas sigue siendo limitada [4].Estos desafíos destacan la complejidad de la ingeniería de líneas celulares, pero las posibles recompensas la convierten en una vía prometedora para reducir costos. A continuación, exploraremos estrategias de optimización de medios.
2. Optimización de Medios y Factores de Crecimiento
Reducir los costos de los medios de cultivo es una estrategia clave para hacer que la carne cultivada sea más asequible. En este momento, los medios de cultivo celular son el mayor gasto en producción de carne cultivada [5][3]. Al reducir estos costos, hay una gran oportunidad de acercar los precios a lo que los consumidores están dispuestos a pagar.
Para alcanzar un precio objetivo de £8 por kilogramo, los costos de los medios deben reducirse en más del 99.9% desde sus niveles actuales de grado farmacéutico. Los factores de crecimiento por sí solos tendrían que limitarse a solo £0.80 por kilogramo [3][5].Como explica el Good Food Institute:
"El mayor desafío que enfrenta la industria de la carne cultivada no es simplemente prescindir de componentes animales en los medios de cultivo celular, sino descubrir cómo hacerlo de manera asequible y cómo optimizar formulaciones asequibles para maximizar la productividad" [3].
Potencial de Reducción de Costos
Uno de los principales enfoques para reducir costos es reemplazar ingredientes costosos de grado farmacéutico por alternativas más baratas de grado alimenticio. Por ejemplo, la albúmina, que representa el 96.6% de las necesidades de proteínas recombinantes, está siendo objeto de sustitutos a base de plantas como el colza y los garbanzos. Asimismo, las empresas están intercambiando aminoácidos individuales por hidrolizados vegetales más asequibles [5][3][1].
Ya se están logrando avances.En agosto de 2024, Believer Meats introdujo un medio libre de componentes animales que cuesta solo £0.50 por litro [6]. Utilizando métodos de fabricación continua como la filtración por flujo tangencial, su análisis mostró que el pollo cultivado podría producirse a £5 por libra en una instalación de 50,000 litros, lo que lo hace competitivo con los precios del pollo orgánico [6]. De manera similar, Mosa Meat, en asociación con Nutreco, demostró que cambiar de aminoácidos de grado farmacéutico a aminoácidos de grado alimentario podría reducir costos en un factor de 100, todo sin sacrificar el rendimiento celular [1].
Plazo de Implementación
En comparación con la ingeniería de líneas celulares, la optimización de medios puede ofrecer resultados mucho más rápido.Mientras que el desarrollo de nuevas líneas celulares puede llevar de 6 a 18 meses [3], reformular medios a menudo aprovecha las cadenas de suministro de grado alimenticio existentes, acelerando el proceso. Susanne Wiegel, Jefa del Programa de Proteínas Alternativas en Nutreco, lo resume bien:
"Alimentar células no es tan diferente de alimentar animales. La mayoría de los nutrientes se proporcionan a través de cultivos agrícolas" [1].
Desafíos Técnicos
A pesar de la promesa de ahorros de costos, el uso de ingredientes de grado alimenticio conlleva desafíos. Estos ingredientes pueden introducir impurezas, inconsistencias en los lotes y posibles impactos en el rendimiento celular y la calidad del producto [5][2]. Además, aumentar la producción para satisfacer la demanda no es una tarea fácil.Capturar solo el 1% del mercado global de carne requeriría millones de kilogramos de albúmina recombinante, superando con creces los niveles de producción actuales para muchas enzimas industriales [5].
A continuación, exploraremos cómo las mejoras en los bioreactores y los procesos pueden reducir aún más los costos.
sbb-itb-c323ed3
3. Mejoras en Bioreactores y Procesos
Después de refinar la ingeniería de líneas celulares y optimizar los medios, el siguiente paso para reducir los costos de la carne cultivada radica en mejorar los bioreactores y los procesos de producción. Mientras que las líneas celulares y los medios se centran en el lado biológico, los sistemas físicos - bioreactores y flujos de trabajo de fabricación - juegan un papel crucial en hacer que la carne cultivada sea más asequible. Como afirma acertadamente el Good Food Institute:
"El diseño del bioproceso es la clave para desbloquear la producción a gran escala de carne cultivada" [3].
En este momento, la mayoría de los biorreactores utilizados en la producción de carne cultivada están adaptados de la industria farmacéutica. Estos sistemas están diseñados para salidas de alto valor y bajo volumen, lo cual no es ideal para las demandas de producción de alimentos que son rentables y de alto volumen [3]. Para competir con la carne tradicional, la industria necesita biorreactores diseñados específicamente para la producción económica a gran escala. Aquí es donde las optimizaciones de procesos pueden ayudar a reducir aún más los costos.
Potencial de Reducción de Costos
Una de las formas más prometedoras de reducir costos es pasando de estándares de producción de grado farmacéutico a estándares de grado alimentario. A diferencia de las aplicaciones farmacéuticas, la carne cultivada solo necesita cumplir con los estándares de seguridad alimentaria, que son menos estrictos. Este cambio podría reducir significativamente los gastos operativos [3].
La eficiencia del proceso es otro factor crítico.Técnicas como el reciclaje de medios de cultivo, la reutilización de flujos de desechos y la implementación de automatización pueden ayudar a minimizar el uso de insumos costosos [3]. Por ejemplo, en septiembre de 2023, Upside Foods anunció sus planes para una instalación a escala comercial cerca de Chicago. Esta instalación tiene como objetivo producir 13,000 toneladas de carne cultivada anualmente utilizando biorreactores de hasta 100,000 litros [1]. Kevin Kayser, el Director Científico de la empresa, destacó la importancia de centrarse en los insumos de materia prima:
"Una de las razones por las que fui contratado fue por los insumos de materia prima... Cuando comencé, estaba en la parte superior de la lista" [1].
Escalabilidad
Escalar los biorreactores es esencial para lograr paridad de precios con la carne convencional. Actualmente, las instalaciones a escala piloto utilizan biorreactores que van de 100 a 1,000 litros.Sin embargo, los análisis tecnoeconómicos sugieren que lograr precios competitivos requerirá biorreactores con volúmenes de 20,000 litros o más - posiblemente incluso 100,000 litros [3][1][2]. Para finales de 2024, al menos una empresa había escalado con éxito a biorreactores con una capacidad de 15,000 litros [3].
La industria está pasando por fases distintas: desde la investigación a escala de banco (biorreactores de menos de 10 litros), hasta pruebas a escala piloto, y eventualmente a producción a escala industrial. Cada etapa exige no solo equipos más grandes, sino también innovaciones en mezcla, suministro de oxígeno y sistemas de monitoreo [3].
Desafíos Técnicos
Escalar biorreactores no está exento de desafíos.Los bioreactores más grandes presentan dificultades técnicas únicas, como la gestión de fuerzas de cizallamiento durante la mezcla y la oxigenación, que pueden dañar células delicadas [3]. La transferencia de oxígeno se vuelve cada vez más compleja a medida que crecen los volúmenes de los bioreactores, y mantener la esterilidad en instalaciones a gran escala y de grado alimenticio es crítico; cualquier contaminación podría resultar en pérdidas significativas de producción [3].
Como señaló Kevin Kayser, la industria está explorando nuevos territorios:
"Cuando comienzas a hablar de 100,000 L o más, no sé si eso va a requerir algún cambio en el medio. No hemos llegado a ese nivel" [1].
A diferencia de la optimización de medios, que puede aprovechar las cadenas de suministro de alimentos existentes, escalar bioreactores requiere resolver problemas de ingeniería completamente nuevos, especialmente a estas tamaños sin precedentes [3].
Plazo de Implementación
Construir instalaciones a escala industrial es un proceso que requiere mucho tiempo y capital. Mientras que desarrollar una nueva línea celular puede tardar de 6 a 18 meses [3], construir y poner en marcha una instalación de producción a gran escala lleva años de planificación y una inversión sustancial [3]. Sin embargo, nuevas tecnologías están ayudando a acelerar las cosas. Por ejemplo, se ha demostrado que los sistemas automatizados y basados en la nube reducen los ciclos de desarrollo en un 25% y mejoran las tasas de éxito en la escalabilidad en un 30% [7]. Chris Williams, CEO de Culture Biosciences, explicó:
"El cambio hacia el bioprocesamiento modular y basado en la nube está acelerándose en los sectores de biotecnología y biofarmacéutica... Ofrece una solución flexible y rentable para equipos que requieren ciclos de desarrollo más rápidos y escalabilidad" [7].
El proceso de cultivo en sí - desde el banco de células hasta la cosecha - generalmente toma de 2 a 8 semanas, dependiendo del tipo de carne que se esté produciendo [3]. Los avances en bioprocesamiento serán críticos para hacer de la carne cultivada una opción competitiva en el mercado.
Comparando los Tres Enfoques
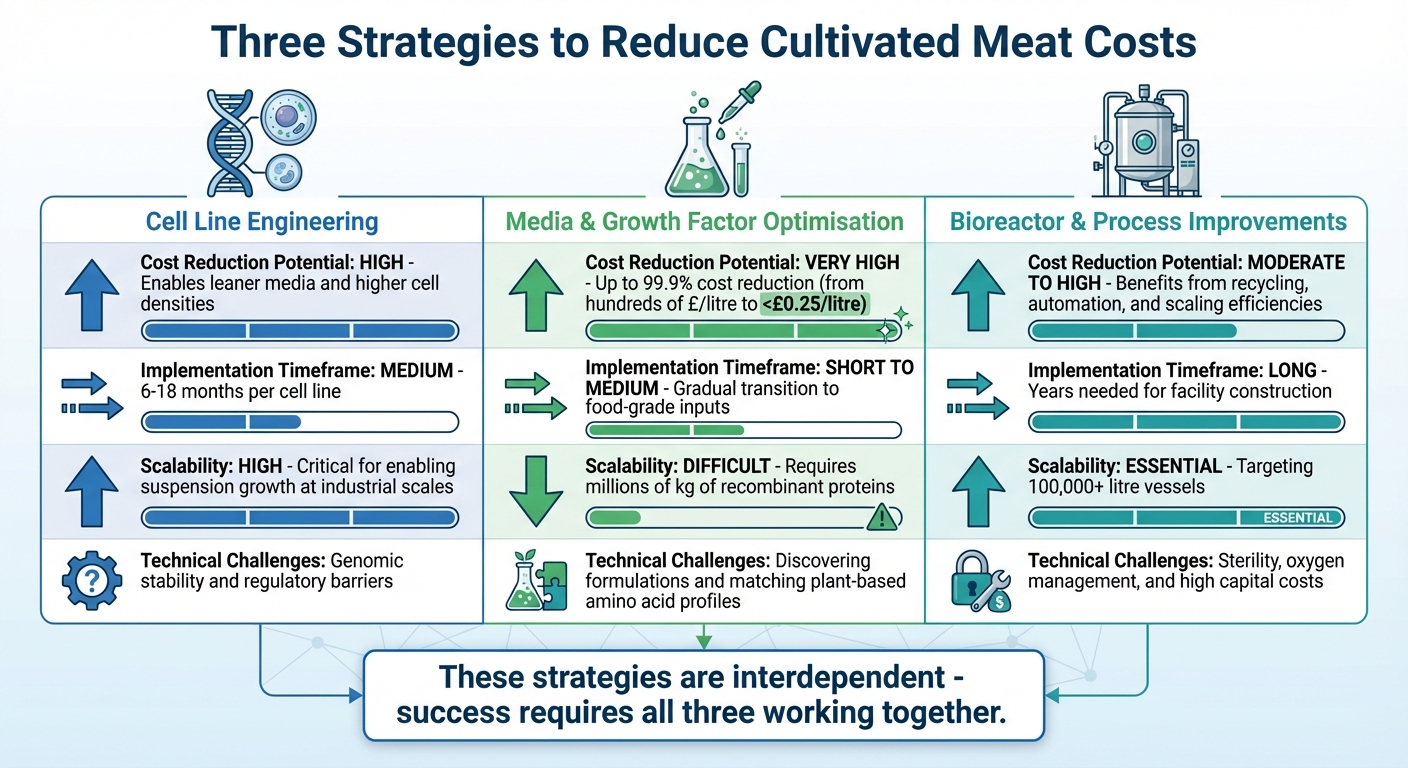
Comparando Tres Estrategias para Reducir los Costos de Producción de Carne Cultivada
Al observar la ingeniería de líneas celulares, la optimización de medios y los avances en biorreactores lado a lado, se revela cuán interconectadas están estas estrategias. Cada una aporta sus propias fortalezas y obstáculos, pero juntas crean un camino para reducir los costos en la producción de carne cultivada.
A continuación se presenta un desglose de cómo se comparan estos enfoques en cuatro criterios clave:
| Criterio | Ingeniería de Líneas Celulares | Optimización de Medios &y Factores de Crecimiento | Mejoras en Bioreactores &y Procesos |
|---|---|---|---|
| Potencial de Reducción de Costos | Alto – permite medios más eficientes y mayores densidades celulares | Muy Alto – podría reducir costos hasta en un 99%.9% de los precios biomédicos actuales | Moderado a Alto – beneficios de reciclaje, automatización y eficiencias de escalado |
| Plazo de Implementación | Medio – generalmente toma de 6 a 18 meses por línea celular | Corto a Medio – implica una transición gradual a insumos de grado alimenticio | Largo – se necesitan años para la construcción y puesta en marcha de la instalación |
| Escalabilidad | Alta – crítica para permitir el crecimiento en suspensión a escalas industriales | Difícil – requiere la producción de millones de kilogramos de proteínas recombinantes | Esencial – apuntando a recipientes de más de 100,000 litros para producción a gran escala |
| Desafíos Técnicos | Estabilidad genómica y barreras regulatorias | Descubrir formulaciones y hacer coincidir perfiles de aminoácidos de origen vegetal | Asegurando la esterilidad, la gestión del oxígeno y el manejo de altos costos de capital |
Cada estrategia desempeña un papel distinto en el abordaje de los desafíos de costos de la carne cultivada.
La optimización de medios se destaca por su potencial inmediato para reducir costos. Los precios podrían caer de cientos de libras por litro a menos de £0.25 por litro [3]. Sin embargo, escalar este enfoque para satisfacer las demandas industriales es un obstáculo significativo.
La ingeniería de líneas celulares, por otro lado, sienta las bases para el éxito. Al permitir el crecimiento en suspensión y reducir los requisitos de medios, apoya tanto la optimización de medios como el escalado de biorreactores [3]. Sin líneas celulares confiables, el progreso en las otras áreas se detendría.
Las mejoras en biorreactores son un juego a largo plazo. Desarrollar y poner en marcha instalaciones capaces de manejar recipientes de 100,000 litros es una tarea desalentadora, pero es esencial para escalar a una producción a nivel de mercancía [3].Los desafíos de ingeniería aquí, particularmente en torno a la esterilidad y la transferencia de oxígeno, siguen siendo un territorio en gran medida inexplorado a esta escala.
La realidad es que ningún enfoque único puede soportar el peso de la reducción de costos por sí solo. Estas estrategias son profundamente interdependientes. Por ejemplo, los medios asequibles solo tienen valor si los biorreactores pueden operar a altos volúmenes, y los biorreactores a gran escala solo tienen sentido si los medios que utilizan son rentables [3]. Juntos, estos esfuerzos crean un marco cohesivo que es crítico para hacer que la carne cultivada a escala comercial sea una realidad.
Conclusión
La ingeniería de líneas celulares juega un papel clave en el impulso del éxito tanto de la refinación de medios como de los avances en biorreactores. Al desarrollar células que crecen más rápido, alcanzan densidades más altas y funcionan bien en medios más ligeros, reduce significativamente los costos asociados con nutrientes y capacidad de biorreactores. Esto lo convierte en un pilar fundamental para reducir los gastos de producción.
La refinación de medios ofrece ahorros inmediatos, con el potencial de reducir los costos de medios hasta en un 99.9%, llevando los precios de grado farmacéutico a menos de £0.20 por litro [3]. Sin embargo, estos ahorros dependen de líneas celulares que puedan prosperar en medios tan rentables. Al mismo tiempo, los diseños avanzados de biorreactores allanan el camino para la producción a gran escala, pero su viabilidad económica depende de emparejarlos con medios asequibles y líneas celulares resistentes y diseñadas.
La línea de tiempo para lograr la paridad de precios con la carne convencional premium en el Reino Unido estará determinada por la rapidez con la que estas tres estrategias - ingeniería celular, desarrollo de medios y escalado de biorreactores - avancen juntas. El progreso en estas áreas formará la base para hacer que la carne cultivada sea más accesible.
Para los consumidores del Reino Unido, la disponibilidad generalizada también dependerá de la aprobación regulatoria, que aún está bajo revisión a finales de 2025 [3], y la creación de instalaciones de producción a gran escala. Las empresas ya están planeando biorreactores de 100,000 litros y apuntando a instalaciones capaces de producir hasta 13,000 toneladas anualmente [1], lo que indica que la infraestructura necesaria está tomando forma.
El camino hacia la carne cultivada asequible dependerá de la integración fluida de estas tres estrategias. Un ecosistema de producción que combine células diseñadas, medios de bajo costo y biorreactores a escala industrial determinará cuándo la carne cultivada pasará de experiencias gastronómicas de nicho a ofertas cotidianas en los supermercados.
Preguntas Frecuentes
¿Cómo ayuda la tecnología de líneas celulares a reducir el costo de la carne cultivada?
Los avances en la tecnología de líneas celulares han reducido el costo de producción de carne cultivada al mejorar el rendimiento de las células utilizadas en el proceso. Estas líneas celulares diseñadas especialmente crecen rápidamente, pueden prosperar en entornos densos y soportar condiciones difíciles como bajos niveles de oxígeno y estrés mecánico. Esto significa menos dependencia de medios de cultivo costosos y una producción más eficiente y de alto rendimiento en biorreactores.
Al reducir los costos de materias primas y procesamiento, la tecnología de líneas celulares está ayudando a hacer la carne cultivada más accesible. Este progreso es un paso hacia su establecimiento como una alternativa práctica a la carne tradicional.
¿Cuáles son los principales desafíos en el uso de medios de grado alimenticio para la producción de carne cultivada?
Cambiar a medios de grado alimenticio para producir carne cultivada conlleva algunos desafíos difíciles.Uno de los mayores obstáculos es el costo. En este momento, los medios ricos en factores de crecimiento - esenciales para el crecimiento celular - representan más de la mitad de los gastos de producción. Para reducir costos, los fabricantes necesitan cambiar de ingredientes de grado farmacéutico caros a alternativas más baratas y compatibles con alimentos. Pero aquí está el problema: desarrollar estas opciones asequibles, ya sea a través de fermentación de precisión o métodos basados en plantas, todavía está en sus primeras etapas y requiere mucha inversión.
Otro problema importante radica en cumplir con estrictas normas de seguridad alimentaria. Los medios de grado alimentario deben ser producidos en condiciones estériles, libres de cualquier contaminante, y cumplir con las regulaciones alimentarias de la Unión Europea. Esto añade capas de complejidad a las cadenas de suministro y a los procesos de control de calidad. Además, eliminar el suero - comúnmente utilizado en medios de grado de investigación - crea nuevos desafíos en la gestión de residuos.Sin el suero actuando como un amortiguador natural, la acumulación de subproductos se convierte en un problema, exigiendo sistemas avanzados de reciclaje o eliminación.
También está el problema de la adaptación celular. Muchas líneas celulares, desarrolladas originalmente para entornos basados en suero, tienen dificultades para crecer en medios químicamente definidos y libres de animales. Esto puede llevar a un crecimiento más lento o células más débiles, a menudo requiriendo ajustes genéticos en las líneas celulares o la creación de suplementos especializados. Abordar estos desafíos es fundamental para escalar la producción de carne cultivada y hacerla más asequible y accesible para los consumidores. Si tienes curiosidad por aprender más sobre este fascinante campo, el
¿Cómo ayudan los bioreactores a gran escala a hacer que la carne cultivada sea más asequible?
Los bioreactores a gran escala, especialmente aquellos con capacidades que superan los 20,000 litros, juegan un papel clave en la reducción de los costos de producción de carne cultivada.Estos sistemas permiten la producción de grandes cantidades de carne, lo que ayuda a distribuir los gastos como equipo, mano de obra y medios de cultivo sobre una mayor producción. Este enfoque ayuda a lograr economías de escala, acercando la carne cultivada al precio de la carne tradicional.
Con este nivel de producción, los fabricantes pueden reducir drásticamente el costo por kilogramo, allanando el camino para que la carne cultivada se convierta en una opción más asequible y viable para los consumidores.













